- 1. Глобални терет рака грлића материце и изазови скрининга
Рак грлића материце остаје главни глобални изазов јавног здравља, упркос томе што се у великој мери може спречити ефикасним скринингом и раном интервенцијом. Према подацима Светске здравствене организације (СЗО), процењених 662.000 нових случајева и 349.000 смртних случајева догодило се широм света у 2022. години, што га сврстава на четврто место по учесталости рака и четврти водећи узрок смртности од рака код жена. Терет болести је несразмерно концентрисан у земљама са ниским и средњим приходима (ЗСНП), где су стопе инциденције и смртности знатно веће него у земљама са високим приходима. То је првенствено последица недостатка висококвалитетних програма скрининга и ефикасног откривања и лечења преканцерозних лезија, што је погоршано:
-Одсуство или слаба инфраструктура за скринингНедостатак приступачних, квалитетних услуга скрининга.
-Ограничења ресурсаОграничена лабораторијска инфраструктура, логистика хладног ланца и поуздана електрична енергија.
-Недостатак радне снагеНедостатак обученог лабораторијског и клиничког особља.
-Кашњења и губитак праћењаВременско кашњење између прикупљања узорка и доступности резултата, што доводи до кашњења у клиничком лечењу или губитка пацијената из праћења[1].
2. Етиологија и молекуларна основа карциногенезе грлића материце
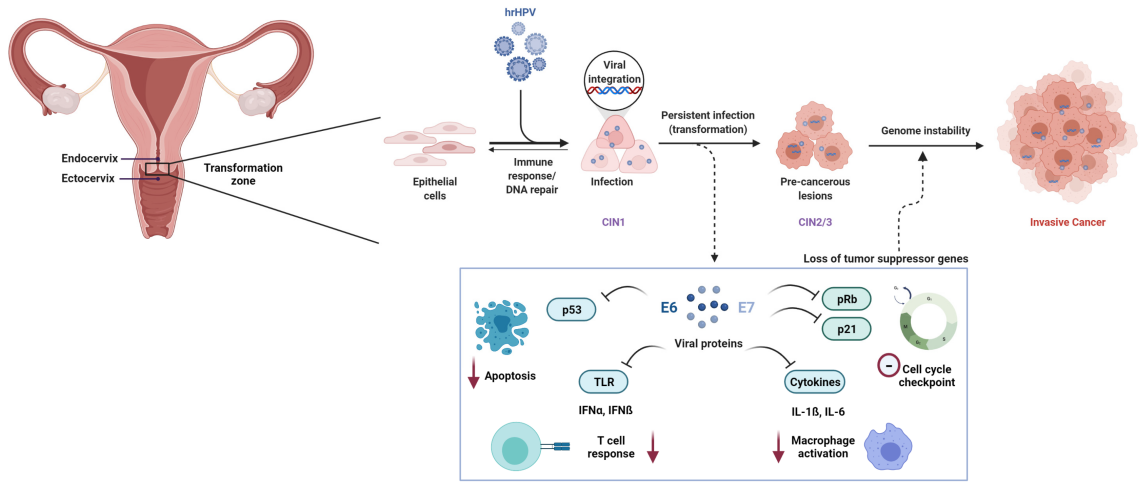
Упорна инфекција високоризичним хуманим папилома вирусом (HR-HPV) је неопходан узрок рака грлића материце. Међу више од 200 идентификованих HPV генотипова, најмање12 врстакласификоване су као канцерогене (Група 1) од стране Међународне агенције за истраживање рака (IARC).

На молекуларном нивоу, канцерогенезу посредовану ХПВ-ом првенствено покрећу вирусни онкопротеини Е6 и Е7. Е6 промовише разградњу тумор супресорског протеина п53, док Е7 функционално инактивира протеин ретинобластома (Rb), што доводи до дисрегулације ћелијског циклуса и малигне трансформације.
3.Стратегије скрининга које препоручује СЗО
Светска здравствена организација препоручује тестирање нуклеинских киселина (NAT) на ХПВ као преферирану примарну методу скрининга за превенцију рака грлића материце.
Општа популација:ХПВ ДНК или мРНК НАТ-ови
Жене које живе са ХИВ-ом:НАТ-ови засновани на ХПВ ДНК
Интервали скрининга:
Жене старости 30–65 година: Сваких 5–10 година
Жене које живе са ХИВ-ом: Сваких 3–5 година
У поређењу са методама заснованим на цитологији, тестирање на ХПВ показујевећа осетљивости пружасупериорна негативна предиктивна вредност, што омогућава дуже и исплативије интервале скрининга.
4.Профил циљног производа СЗО за тестове за скрининг ХПВ-а
СЗО је развилаПрофил циљног производа (TPP)за ХПВ скрининг тестове намењене за употребу у децентрализованим условима и условима са ограниченим ресурсима.[1]
Кључне карактеристике укључују:
- Компатибилност са самостално прикупљеним узорцима
- Детекција вишеструких генотипова ХПВ високог ризика (≥12 типова)
- Руковање од стране особља које није обучено за рад у лабораторији
- Резултати доступни у оквиру једног клиничког сусрета
Ови критеријуми подржавају тестирање на месту пружања неге и стратегије „скрининга и лечења“.
5.Потпуно аутоматизована платформа за детекцију високоризичног ХПВ-а
Систем AIO800 компаније Macro & Micro-Test пружапотпуно аутоматизован ток рада од узорка до одговораинтегришући екстракцију, амплификацију и детекцију нуклеинских киселина у складу са стратегијама скрининга које препоручује СЗО.

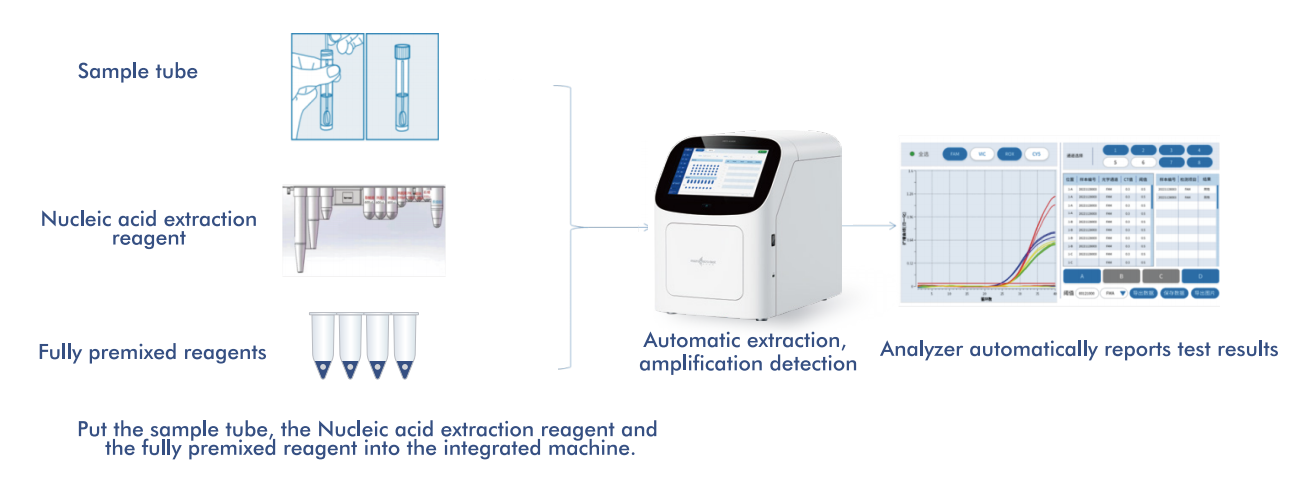
5.1 Аутоматизовани ток рада од узорка до одговора
Платформа интегрише екстракцију, амплификацију и детекцију нуклеинских киселина у јединствен, затворени систем, захтевајући минималну интервенцију оператера. Овај дизајн:
- -Смањује зависност од специјализованог лабораторијског особља
- -Минимизира варијабилност процеса и ризик од контаминације
- -Омогућава примену у децентрализованим здравственим установама
Истовремено, његов пропусни капацитет подржава примену у централизованим лабораторијама, олакшавајући програме скрининга великих размера.
5.2 Широка покривеност генотипизације
Систем детектује 14 високоризичних типова ХПВ-а, укључујући свих 12 канцерогених типова класификованих од стране IARC-а (ХПВ16, 18, 31, 33, 35, 39, 45, 51, 52, 56, 58 и 59), као и ХПВ66 и ХПВ68.
Важно је да пружагенотипизација специфична за типрезултате, омогућавајући стратификацију ризика и прецизније клиничко управљање.
5.3 Аналитичка осетљивост и клиничке импликације
Са границом детекције од 300 копија/мл, систем је способан да идентификује ХПВ инфекцију ниског нивоа која доприноси:
- -Раније откривање клинички релевантних инфекција
- -Побољшана негативна предиктивна вредност
- -Подршка за продужене интервале скрининга
5.4 Подршка за самостално узорковање
Платформа је компатибилна са обаузорци бриса грлића материце и самоприкупљени узорци уринаусклађивање са препорукама СЗО за решавање кључних препрека за прихватање скрининга, укључујући:
- -Ограничен приступ здравственим установама
- -Социокултурна ограничења
Време објаве: 27. март 2026.
